

![[DIGITALE BIBLIOTHEK DER FES]](/images/digbib/d_digbib.gif)

TEILDOKUMENT:
[Seite der Druckausg.: 47]
Rolf Kreienberg
Flächendeckende qualitätsorientierte onkologische Versorgung in der Bundesrepublik Deutschland
Gesundheitspolitiker, Krankenkassen, Kassenärztliche Bundesvereinigung und Bundesärztekammer, wissenschaftliche Fachgesellschaften und nicht zuletzt die Patientinnen und Patienten fordern eine flächendeckende qualitätsgesicherte onkologische Versorgung in unserem Lande.
Aus Sicht jedes einzelnen Teilbereiches unseres Gesundheitssystems werden in der onkologischen Versorgung unterschiedliche Anforderungen an diese Qualität gestellt.
Es gilt, alle Leistungsträger im System gleichermaßen über die Defizite zu informieren und gemeinsam nach realisierbaren Lösungsansätzen zu suchen, um die Versorgungsqualität flächendeckend zu sichern bzw. zeitnah allen Patientinnen und Patienten zur Verfügung zu stellen.
Am Beispiel des Mammakarzinoms, als eine der grossen Tumorerkrankungen in unserer Bevölkerung, sind die Versorgungsqualität und die Möglichkeiten zu deren Verbesserung dargestellt.
Bei 42 Millionen Frauen in der Bundesrepublik erkranken jährlich 53.000 neu am Mammakarzinom. An dieser Erkrankung sterben jährlich18.000 Frauen. Insgesamt versterben 36 % der Patientinnen an ihrer Erkrankung. Die Rate an Mammakarzinompatientinnen steigt pro Jahr um etwa 1 %, die Sterblichkeit ist unverändert. Die Ursachen für den Anstieg der Erkrankungen sind unbekannt.
In den USA stieg die Erkrankungsrate von 1940 – 1982 ebenfalls um 1 % pro Jahr, von 1982 – 1987 um 4 %. Von 1990 – 1994 ist der Anstieg auf
[Seite der Druckausg.: 48]
0,2 % pro Jahr zurückgegangen. Von 1940 – 1985 war die Sterblichkeit in den USA unverändert. 1990 – 1994 sank sie um jährlich 2 %. (1)
Der Anstieg der Erkrankungsrate beschränkte sich in den USA auf Tumoren unter 2 cm. Die Tumorgröße bei Erstdiagnose sank zwischen 1988 – 1994 um 7,4 %.
Die sinkende Sterblichkeit wird in den USA auf
- die Einführung eines Brustkrebsfrüherkennungsprogramms,
- die konsequente Durchführung der medikamentösen postoperativen Therapie und
- die Bestrahlung nach radikaler Brustoperation zurückgeführt.
So konnte gezeigt werden, dass durch die jährliche Mammographie im Alter zwischen 50 und 74 die Mortalität um 26 % sinkt. Ursache hierfür ist die Erkennung des nichttastaberen Karzinoms zu einem frühstmöglichen Zeitpunkt, d.h. vor der bereits stattgefundenen systemischen Ausbreitung bzw. in einem prognostisch günstigerem Stadium. (2)
Auch bei jüngeren Frauen zwischen 40 und 49 Jahren sinkt die Mortalität durch die jährliche Früherkennungsmammographie um 17 %. Der außerordentlich günstige Effekt durch die Früherkennungsmammographie tritt jedoch erst nach 10 bis 15 Jahren auf. Nach diesem Zeitraum wird er erst statistisch signifikant. (3)
Bei einer Meta-Analyse mit 18.000 medikamentös behandelnden Frauen aus 47 Studien konnte gezeigt werden, dass durch die konsequente Durchführung der Chemotherapie im Anschluss an die durchgeführte Mammakarzinom-Operation die Mortalität bei Frauen unter 50 um 27 % und bei Frauen über 50 Jahren um immerhin 11 % gesenkt werden kann. (4)
Eine dänische Arbeitsgruppe um Overgaard konnte zeigen, dass, bei 1708 prämenopausalen Frauen mit Brustkrebs im Stadium II oder III, nach der radikalen Entfernung der Brust und einer adjuvanten Chemotherapie mit zusätzlicher Bestrahlung nach 10 Jahren 9 % mehr Frauen lebten, als wenn nur Chemotherapie verabfolgt wurde. (5)
Diese beispielhaften Zahlen zeigen, dass durch konsequente Früherkennung und durch konsequent durchgeführte Therapien, insbesondere in der
[Seite der Druckausg.: 49]
Fläche, sowohl die Erkrankungsraten an Mammakarzinom, als auch die Sterberaten gesenkt werden können.
Für die Bundesrepublik Deutschland existieren solche Zahlen nicht. Die bisher auf der Basis der Register des Saarlandes und der ehemaligen DDR bekannten Zahlen und die dementsprechenden Hochrechnungen zeigen ansteigende Inzidenzzahlen und stagnierende Sterblichkeitsraten für die heutige Bundesrepublik, die den Erfolgsmeldungen europäischer Nachbarländer und auch denen der USA nicht standhalten.
Hierzu einige Einzeldaten aus einer Münchener Feldstudie zur Therapie des Mammakarzioms (6), die die Unterschiede zwischen BRD und den USA besonders verdeutlichen. (Abb. 1)
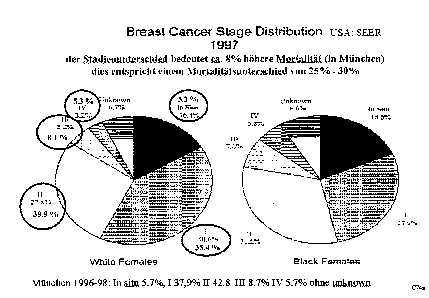
Abbildung 1:
(vergroessertes Bild laden)
[Seite der Druckausg.: 50]
Vergleicht man die diagnostizierten Stadien bei weissen Frauen in den USA mit denen der Münchener Bevölkerung, so fällt auf, dass die Anteile der Vorstadien, d.h. in situ Karzinome, die in den USA bzw. in München diagnostiziert werden, stark differieren. In den USA befinden sich 16,4 % der Patientinnen in diesem Vorstadium, während es in München nur 5,3 % sind. Im Stadium I der Erkrankung finden sich in München 35,4 %, in den USA 40,6 %, im Stadium II 39,9 % in München, 27,8 % in den USA, im Stadium III 8,1 % in München, 5,2 % in den USA und im Stadium IV 5,3 % in München, 3,2 % in den USA. Die Patientinnen befinden sich also bei der Erstdiagnose in der Bundesrepublik in einem deutlich späteren Stadium. Dieser Stadienunterschied bedeutet in München eine 8 %ige höhere Mortalität als in den USA, was einem Mortalitätsunterschied von 25 bis 30 % entspricht.
Dass, neben der in der BRD nicht durchgeführten Früherkennung, die die Ursache für diesen obengenannten Stadienunterschied darstellt, auch unterschiedliche meist nicht standardisierte Therapiestrategien zu zusätzlichen Qualitätsverlusten und damit zur höheren Mortalität bzw. Lebensqualitätsverlusten führen, ist bekannt. Die Daten aus München zeigen, dass, trotz einer Tumorgröße unter 2 cm und eines G2 Tumors bei einem Alter unter 70 Jahren, der Anteil der Radikaloperationen gegenüber der Brust erhaltenden Therapie zwischen 5 und 55 % schwankt. (6) (Abb. 2)
[Seite der Druckausg.: 51]
Abbildung 2:
(vergroessertes Bild laden)
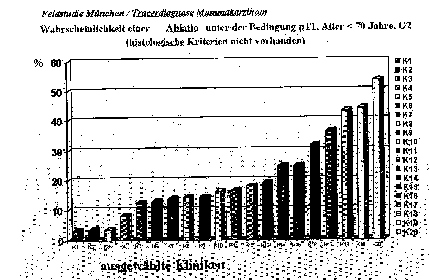
Aus anderen Umfragen ist bekannt, dass ca. 1/3 aller Patientinnen mit Mammakarzinom eine nicht suffiziente oder eine nicht optimal angepasste adjuvante Therapie erhalten und durch diese Therapievariationen ein weiterer Qualitätsverlust hingenommen werden muss. Therapieleitlinien, die eine optimale Therapie für die verschiedenen Stadien und Prognosefaktoren beim Mammakarzinom empfehlen, werden nur von 80 % der Therapeuten gekannt, nur zu ca. 80 % den Patientinnen weiterempfohlen und wahrscheinlich auch nur von 80 % der Patientinnen befolgt. Dieses Rechenbeispiel zeigt, dass wahrscheinlich nur jede zweite Patientin die Therapie erhält, die leitlinienentsprechend ausgewählt ist und damit optimale Ergebnisse erbringen könnte.
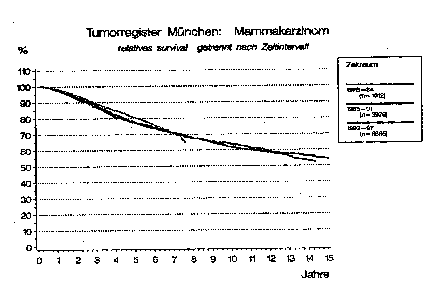
Die Überlebenskurven für das Mammakarzinom im Tumorregister München getrennt für die Zeiträume 1978 – 1984, 1985 – 1991 und 1992 – 1997 zeigen keinen Überlebensgewinn für diese Tumorentität. Schlüsselt man diese Überlebenskurven für die verschiedenen Tumordurchmesser und die genannten Jahre getrennt auf, so zeigt sich sogar, dass für die fortgeschrit-
[Seite der Druckausg.: 52]
tenen Tumoren die Therapieergebnisse in den Jahren 1992 – 1997 schlechter werden als in den Jahrgängen zuvor. (Abb. 3, 4)
Abbildung 3:
(vergroessertes Bild laden)
[Seite der Druckausg.: 53]
Abbildung 4:
(vergroessertes Bild laden)
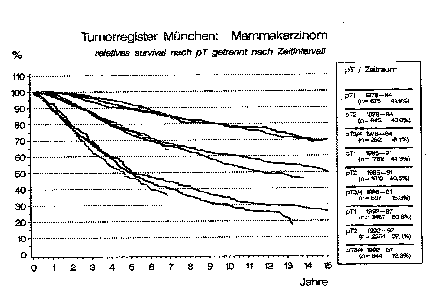
Ursache hierfür ist sicher, dass die guten Ergebnisse von Hochleistungszentren in unserer Republik dadurch verschlechtert werden, dass in der Fläche ein nicht unerheblicher Anteil der Patientinnen nicht leitliniengerecht behandelt, unter- oder übertherapiert werden, nicht die adäquate Operation, die richtige Zusammenstellung der für das Erkrankungsstadium notwendigen Chemotherapiekombinationen bzw. eine adäquate Strahlentherapie erhält.
In der Zusammenschau der leistungsstarken Abteilungen mit den Abteilungen geringerer Leistungsdichte resultieren somit unverändert schlechte Überlebensdaten, die in Kombination mit mangelnder Früherkennung und der Behandlung späterer Stadien in der Bundesrepublik dazu führen, dass die Sterblichkeit an Mammakarzinom 1996 deutlich höher war als in vergleichbaren europäischen Ländern, mit zum Teil schlechteren Sozialsystemen. Dies kann eigentlich bei den hohen Ausgaben für unser Gesundheits- system einerseits und andererseits im Sinne unserer Patienten nicht hingenommen werden.
[Seite der Druckausg.: 54]
Lösungsvorschläge zur Verbesserung der Versorgungsqualität
Früherkennung, Diagnostik, Therapie und Nachsorge sowie die Behandlung fortgeschrittener Mammatumoren in der Palliativsituation sind ein außerordentliches komplexes Geschehen, das das Zusammenspiel verschiedenster ärztlicher Disziplinen zu den verschiedensten Zeitpunkten auf höchstem Niveau erfordert. Schwache Glieder in der Versorgungskette vermindern die Versorgungsqualität. Will man die Versorgungsqualität verbessern, muss gewährleistet sein, dass jeder mit der Versorgung des Mammakarzinoms Betraute seine individuelle Leistungsqualität dokumentiert, damit im Nachhinein überhaupt festgestellt werden kann, wo, bei nachlassender Qualität im Einzelfall, die Schwachstellen des Systems liegen. (Abb. 5)
Abbildung 5:
(vergroessertes Bild laden)
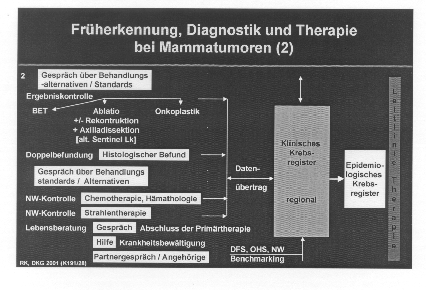
Grundvoraussetzung für die Verbesserung der Versorgungsqualität in der Fläche ist somit das Vorhandensein einer evidenzbasierten Leitlinie zu der Diagnostik, Therapie, Nachsorge und Palliation des jeweiligen Karzinoms, deren Kenntnis durch die verschiedenen Behandler und deren konsequente Umsetzung am und mit dem Patienten. Daneben muss die jeweils vom
[Seite der Druckausg.: 55]
Behandler erbrachte Leistung konsequent in ein klinisches Krebsregister eingegeben werden und für den Patienten, für die behandelnde Klinik, für verschiedene Kliniken der Region und überregional Datensätze zusammengetragen werden, die es ermöglichen, die Qualität im Einzelfall und damit auch ihre Schwachstellen nachvollziehbar und transparent zu machen.
Abbildung 6:
(vergroessertes Bild laden)
Abbildung 6:
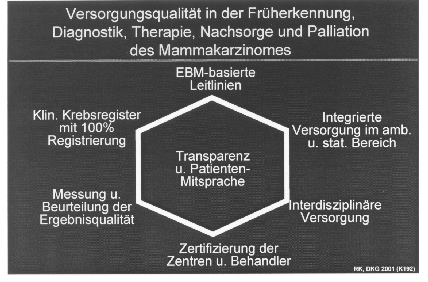
Die Versorgungsqualität in der Früherkennung, Diagnostik, Therapie, Nachsorge und Palliation der onkologischen Erkrankungen kann flächendeckend nur dann verbessert werden, wenn folgende Forderungen erfüllt sind:
- Vorliegen von Leitlinien auf dem Boden der evidence based medicine für Früherkennung, Diagnose, Therapie, Nachsorge und Palliation,
[Seite der Druckausg.: 56]
- vollständige Umsetzung dieser Leitlinien durch die behandelnden Institutionen und im einzelnen die die Behandlung durchführenden Ärzte,
- 100 %-ige Meldung aller Leistungen in klinischen Tumorregistern,
- die Mitteilung der Ergebnisqualität ist für alle onkologisch tätigen Ärzte unabdingbar,
- Zertifizierung von Behandlern und Einrichtungen in regelmässigen Abständen,
- Auflösung der Trennung von ambulanter und stationärer Versorgung, Einführung der integrierten Versorgung.
Flankierend müssen:
- die Patienten in die Lage versetzt werden, das genaue Ausmaß ihrer Erkrankung und die hierfür notwendigen diagnostischen und therapeutischen Schritte zu kennen, zu beurteilen und aktiv an ihrer Behandlung teilzunehmen,
- die Ergebnisse der Zertifizierung von Behandlern und Einrichtungen sowie der Nachweis der Ergebnisqualität sollen zu Incentives bzw. Vergütungsabschlägen bei Nichterfüllung der oben genannten Qualitätsmerkmale und ggf. zu strukturellen Umsetzungen führen.
Wichtig ist, dass alle diese Forderungen nicht nacheinander und isoliert, sondern gleichzeitig von den an der Versorgung beteiligten Gruppen wie Politik, Selbstverwaltung, Leistungserbringer und Patientinnen angegangen und gelöst werden müssen.
Nur eine zeitnahe und gleichzeitige Lösung dieser Forderungen könnte dazu führen, dass auch in unserem Land eine Senkung der Mortalität, eine Steigerung der Lebensqualität möglich ist. Bei der Konzentrierung aller Kräfte ist eine qualitätsgesicherte flächendeckende onkologische Versorgung auch in der BRD möglich. Sie wird dann Ergebnisse erbringen, die die Bundesrepublik wieder in eine Spitzenposition in der Versorgung Krebskranker bringt.
[Seite der Druckausg.: 57]
1. Ries LAG et al. (1997): SEER Cancer Statistics Review, 1973 – 1994, National Cancer Institute
2. Kerlikowske K., Grady D., Rubin S.M., Sandrock C., Ernster V.L. (1995): Efficacy of screening mammography. A meta-analysis. JAMA 273: 149 –54
3. Mettlin C., Smart C.R. (1994): Breast cancer detection guidelines for women aged 40 to 49 years: rationale for the American Cancer Society reaffirmation of recommendations. American Cancer Society. CA Cancer JClin 44: 248 – 55
4. Early Breast Cancer Trialists´ Collaborative Group (1998): Polychemotherapy for early breast cancer: an overview of the randomised trials. Lancet 352: 930 – 942
5. Overgaard Met et (1997): Postoperative radiotherapy in high-risk premenopausal women with breast cancer who receive adjuvant chemotherapy. Danish Breast Cancer Cooperative Group 82b Trial. N Engl J Med. 337: 949 –55
6. Hölzel und Mitarbeiter 2001, Persönliche Mitteilung
[Seite der Druckausg.: 58 = Leerseite]
© Friedrich Ebert Stiftung | technical support | net edition fes-library | Februar 2002